অরবিটাল কাকে বলে? অরবিট ও অরবিটাল এর পার্থক্য
সুপ্রিয় পাঠ বৃন্দ আমাদের ওয়েবসাইটের শিক্ষা রিলেটেড অরবিটাল বিষয়ক উক্ত পোস্টে আপনাদেরকে স্বাগতম। উক্ত পোস্টে আমরা আপনাদেরকে
অরবিটাল কাকে বলে,,, অরবিট ও অরবিটাল কাকে বলে,,, আণবিক অরবিটাল কাকে বলে,,, অরবিট ও অরবিটাল এর পার্থক্য,,, P উপশক্তিস্তরে অরবিটাল কয়টি,,, ইত্যাদি সম্পর্কিত বিভিন্ন তথ্য আলোচনা করার মাধ্যমে জানাচ্ছি।
রসায়নের পর্যায় সারণির বিভিন্ন তথ্য বা পরমাণু নিয়ে আলোচনা করার ক্ষেত্রে অরবিট এবং অরবিটাল উল্লেখযোগ্য। কেননা অরবিট বা অরবিটাল যে সকল পরমাণু বা মৌল নিয়ে আলোচনা করা হয়ে থাকে সেগুলো পর্যায় সারণির ১১৮টি মৌলের মধ্যে বিভিন্ন মৌলসমূহ।
এজন্য রসায়নের বিভিন্ন বিষয়ের পাশাপাশি পর্যায় সারণির বিভিন্ন মৌলের অরবিট কিংবা অরবিটালে অবস্থানরত কক্ষপথ ও অরবিটাল সম্পর্কে জানার প্রয়োজনীয়তা রয়েছে।
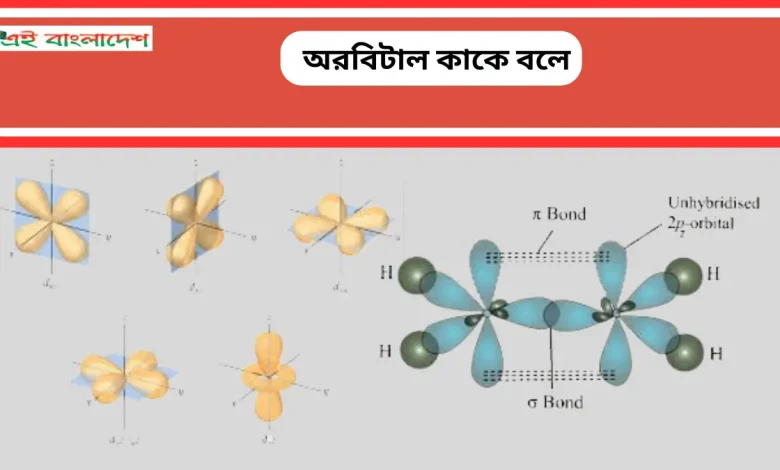
অরবিটাল কাকে বলে
নিউক্লিয়াসের চারদিকে যে অঞ্চলে ইলেকট্রন প্রাপ্তির সম্ভাবনা ৯০ থেকে ৯৫ শতাংশ তাকে অরবিটাল বলা হয়। অর্থাৎ নিউক্লিয়াসের চারদিকে যে এলাকায় আবর্তনশীল ও নির্দিষ্ট শক্তি যুক্ত ইলেকট্রন ম্যাগের অবস্থানের সম্ভাবনা 90 থেকে 95 শতাংশ হয়ে থাকে, ইলেকট্রন ম্যাগের সে এলাকাকে অরবিটাল বলা হয়।
অরবিট ও অরবিটাল কাকে বলে
অরবিট:- পরমাণুতে যে সকল ইলেকট্রন রয়েছে সে ইলেকট্রন গুলো যে সকল কক্ষপথে পরিভ্রমণ করে বা ঘুরতে থাকে যে সকল কক্ষপথকে অরবিট বলা হয়।
অরবিটাল:- নিউক্লিয়াসের চারদিকে যে অঞ্চলে ইলেকট্রন প্রাপ্তির সম্ভাবনা ৯০ থেকে ৯৫ শতাংশ তাকে অরবিটাল বলা হয়।
আণবিক অরবিটাল কাকে বলে
একটি অনুতে ইলেকট্রন সমূহের কেবল একটির পরিবর্তে যদি একাধিক পরমাণু দিয়ে ভাগ করা অরবিটাল গুলো দখল করতে পারে। এ সকল অরবিটাল গুলোকে আণবিক অরবিটাল বলে। অর্থাৎ বিভিন্ন অনুর বিভিন্ন পরমাণু থেকে পারমাণবিক অরবিটাল গুলোর সংমিশ্রণের মাধ্যমে আনবিক অরবিটাল গঠিত হয়।
অরবিট ও অরবিটাল এর পার্থক্য
অরবিট ও অরবিটাল এর মধ্যে পার্থক্যঃ
১. অরবিট, যা নিউক্লিয়াসের চারদিকে সমতলিকভাবে কিংবা দ্বিমাত্রিকভাবে অবস্থান করে থাকে। অরবিটালের ইলেকট্রন ধারণ ক্ষমতা হলো 2n2 ,,, যেখানে, n হলো = কক্ষপথের ক্রমিক সংখ্যা।
এছাড়াও নিউক্লিয়াসের ধনাত্মক যে এনার্জি রয়েছে এবং নিউক্লিয়াসের তাদের পরস্পরিক ক্রিয়ার মাধ্যমে সচল ইলেকট্রনের কৌণিক ভরবেগ কে আবর্তন করলে সেখানে সর্বদা একই থাকে। যার ফলে কক্ষপথ তৈরি হয়।
অপরদিকে অরবিটাল যা পরমাণুর অন্তস্থ যে অনির্দিষ্টকালের অঞ্চল বাসস্থান রয়েছে সেখানে ইলেকট্রন পাওয়ার সম্ভাবনা বেশি।
এছাড়া বিজ্ঞানী হাইজেনবার্গের অনিশ্চয়তার সূত্র থেকে আমরা জানতে পারি যে, একটি নির্দিষ্ট মুহূর্তের জন্য ইলেকট্রনের যে অবস্থান ও গতিবেগ রয়েছে তা একসঙ্গে বলা সম্ভব নয়।
সেজন্য সেখানে এক মুহূর্তে ইলেকট্রন পাওয়ার সম্ভাবনা সবচেয়ে বেশি থাকে, এবং তাকে অরবিটাল বলা হয়। অরবিটালের বাস্তব রূপে পরমাণুর মধ্যে অর্থাৎ নিউক্লিয়াসের চারদিকে ত্রিমাত্রিকভাবে স্থানগুলোকে নির্দেশ করে থাকে।
২. প্রধান কোয়ান্টাম সংখ্যা কিংবা প্রদান শক্তি স্তর অরবিট নামে পরিচিত। অপরদিকে উপশক্তির স্তরের সম্ভাব্য যে অঞ্চল রয়েছে সে অঞ্চল হল অরবিটাল।
৩. অরবিট কে সাধারণত K,L,M,N,O ইত্যাদি দ্বারা প্রকাশ করা হয়ে থাকে। তবে অরবিটালকে S, Px, PY ,PZ ইত্যাদি দ্বারা প্রকাশ করা হয়ে থাকে
৪. একটি অরবিটে সাধারণত সর্বাধিক 2n2 ইলেকট্রন বিদ্যমান থাকতে পারে,,, তবে অর বিড়ালের সর্বাধিক দুটি ইলেকট্রন পর্যন্ত থাকতে পারে।
৫. অরবিট, যা হলো নির্দিষ্ট কক্ষপথ।যেখানে ইলেকট্রন গুলো কেন্দ্র করে ঘুরতে থাকে। তবে অর্পিটাল হলো নিউক্লিয়াসের চারদিকে একটি নির্দিষ্ট স্থান যে স্থানে ইলেকট্রনের আধিককিং বা ইলেকট্রনের পরিমাণ সবচেয়ে বেশি থাকে
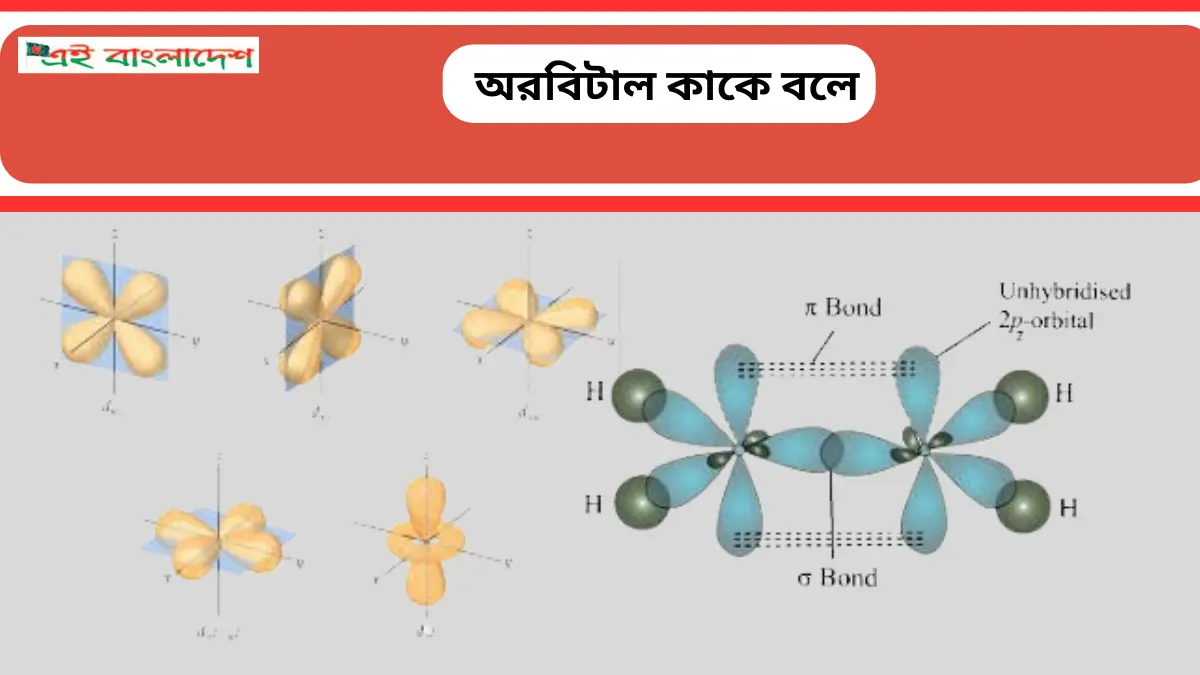
P উপশক্তিস্তরে অরবিটাল কয়টি
p উপস্তরে মোট অরবিটালের সংখ্যা হলো 3,,, p উপস্তরের সহকারী কোয়ান্টাম সংখ্যা কে (l) দ্বারা প্রকাশ করা হয়। সহকারী কোয়ান্টাম সংখ্যার মান P উপশক্তি স্তরে 1,,
যেকোনো একটি পরমানুর ইলেকট্রন বিন্যাস করলে p উপশক্তির স্তরে তিনটি অর্বিতাল বিদ্যমান লক্ষণীয়। p উপশক্তি স্তরে তিনটি অরবিটাল নিয়ে গঠিত। এমন কিছু মৌলের উদাহরণ নিম্নরূপ :-
Na(11) → 1s2, 2s2, 2p6, 3s1
উক্ত পোস্টের মাধ্যমে আমরা আপনাদেরকে অরবিট এবং অরবিটাল সম্পর্কিত বিভিন্ন তথ্য আলোচনা করার মাধ্যমে জানিয়েছি।
আশা করি,, অরবিট এবং অরবিটাল সম্পর্কিত বিভিন্ন তথ্য, সংজ্ঞা এবং অরবিট ও অরবিটাল এর মধ্যে পার্থক্য ইত্যাদি সম্পর্কে যথাযথভাবে জানার মাধ্যমে আপনারা উপকৃত হতে পেরেছেন।



